A Agência Nacional de Vigilância Sanitária ( Anvisa) afirmou hoje (30) que não recebeu, até o momento, nenhum pedido de registro referente à vacina russa, batizada de Sputnik V. Ainda segundo a autarquia, também não há nenhum pedido formal que trate da autorização de pesquisa clínica no Brasil para a vacina em questão.
A Anvisa informou que nesta quinta-feira (29) chegou à agência apenas um e-mail do laboratório União Química, comunicando sobre a apresentação de documentos prévios. Os documentos foram enviados com um pedido para que a agência faça uma análise prévia, antes da apresentação formal do pedido de pesquisa.
Em seu comunicado, o laboratório esclareceu que os detalhes para a pesquisa clínica de fase 3 da Sputnik V ainda serão apresentados em data que depende da União Química. “As informações enviadas não são um pedido formal de autorização para a pesquisa e não são suficientes para a autorização da Anvisa. Na prática, a pesquisa não está autorizada e esse pedido ainda não foi feito pelo laboratório”, explicou a Anvisa, por meio de nota.
A agência acrescentou que a documentação para solicitar a autorização de pesquisa clínica chama-se Dossiê de Desenvolvimento Clínico de Medicamento, que ainda não foi apresentado para a vacina. O laboratório também manifestou interesse em realizar uma reunião de caráter técnico com a Anvisa antes de pedir formalmente a autorização da pesquisa clínica para a Sputnik V.
“A Anvisa tem mantido canal aberto com todas as instituições envolvidas no desenvolvimento de vacinas e medicamentos contra a covid-19. A documentação recebida nesta quinta é parte desta estratégia, mas ainda são documentos prévios e não se trata de pedido de autorização para realizar os estudos em fase 3 (com testes em humanos) ou o pedido de registro”, ressaltou a agência.
Estudos clínicos
A Anvisa lembrou que estudos clínicos são realizados com seres humanos depois de obtidos dados e informações significativos nas etapas anteriores. O protocolo dessa fase precisa ser avaliado e aprovado pela Agência de Vigilância Sanitária antes da sua execução.
Registro
A fase seguinte à de estudos clínicos, é a de registro. Para essa análise, profissionais especializados da Anvisa revisam todos os documentos técnicos e regulatórios e verificam os dados de segurança e eficácia, bem como a qualidade da vacina. O registro, concedido pela Anvisa, é o sinal verde para que a vacina seja comercializada e disponibilizada no país.
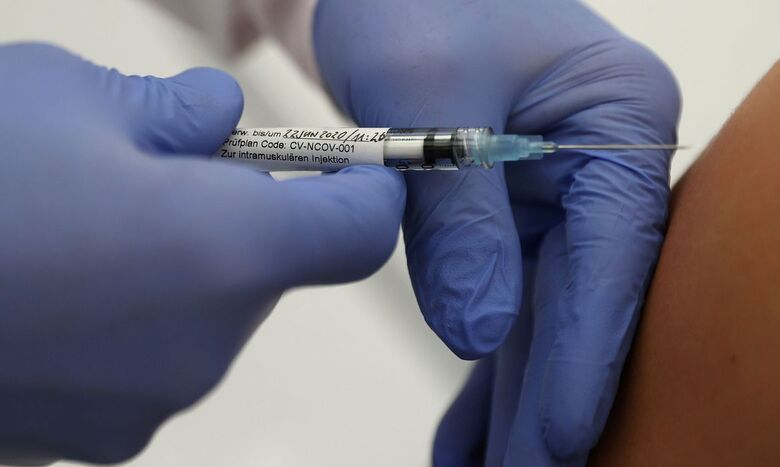 REUTERS/Kai Pfaffenbach/Direitos reservados
REUTERS/Kai Pfaffenbach/Direitos reservados


